用語説明
国際的に受け入れられているガイドラインに沿った試験とは?
安全性試験の結果は、世界中で科学的に受け入れられ、認められることが重要です。そのためには、国際的な安全性試験法ガイドラインに則った試験を行う必要があります。
代表的な安全性試験法ガイドラインには、下記のものがあります。
- OECD(経済協力開発機構)テストガイドライン
- ICH(日・米・EU三極医薬品規制ハーモナイゼーション国際会議)に基づき策定されたガイドライン
- FDA(US Food and Drug Administration)ガイドライン
安全性を確認する試験方法は?
毎日食べ続けても大丈夫か、いろんな場面を想定し、安全性を確認することが重要です。そのために、以下の様な種々の試験を行います。
- 発がん性はないか?:遺伝毒性試験、発がん性試験
- その他の健康への影響はないか?:亜急性毒性試験、慢性毒性試験
- 一度に大量に食べても大丈夫か?:急性毒性試験
- 食べた本人が妊娠しなかったり、生まれた赤ちゃんが妊娠しなくなることはないか?:二世代生殖毒性試験
- 妊娠中に食べたとき胎児への影響はないか?:催奇形性試験
GLP(Good Laboratory Practice)基準とは?
医薬品や食品の安全性を評価する検査や試験が、正確かつ適切に行われたことを保証するための基準です。試験施設の構造設備、標準操作手順書、動物の管理、試験計画書や最終報告書の作成等を細かく規定し、また、信頼性保証部門設置を義務とし、そこが試験内容を確認、適合していることを証明します。公的機関による定期的(3年毎)な適正確認が必要です。
プロテインキナーゼC(蛋白質リン酸化酵素、PKC)活性とは?
プロテインキナーゼC(PKC)は細胞の増殖や分化、アポトーシス等の様々な細胞応答に関与するセリン/スレオニンリン酸化酵素です。活性化したPKCは、基質となる蛋白質をリン酸化することで、基質蛋白質の機能を制御し、外的情報に依存した細胞応答を引き起こすことが知られています。
発がん性を評価する試験
がんが発生するためには、まず遺伝子に異常がおき、正常な細胞が突然変異を起こし、がんの元となる細胞ができる段階(発がんイニシエーション)と、こうした細胞の増殖を促進する段階(発がんプロモーション)の2つが関与すると考えられています(発がん2段階説)。
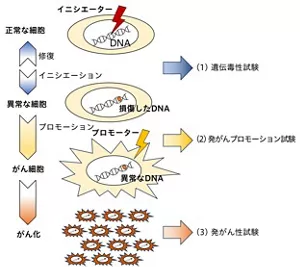
図1 発がんのメカニズム
(1)発がんイニシエーションにより遺伝物質(DNAや染色体など)に障害を与える作用を遺伝毒性といい、遺伝毒性試験により確認します。なお、「遺伝」とありますが、子孫にまで遺伝して影響を及ぼす作用を直接意味する用語ではありません。発がんイニシエーション作用を示すものとしては、放射線、紫外線、カビ毒、たばこに含まれるタールや、焼き魚のコゲなどが知られています。
(2)異常となった細胞の増殖を促進する発がんプロモーション作用は、発ガンプロモーション試験により確認します。発がんプロモーション作用に関しては、高脂肪食、リノール酸、食塩やアスコルビン酸ナトリウム(ビタミンCのナトリウム塩)などの食品成分にもこうした作用があることが報告されています。
(3)実際にがん化するかの確認は、発がん性試験により行います。
(1)遺伝毒性試験とは?
遺伝毒性(変異原性)試験は、発がんの最初の段階である物質による遺伝子およびそれを含む染色体への損傷を短期かつ簡便に検出するのに用いられます。遺伝毒性の有無は、以下の様な複数の試験結果より、総合的に判定します。
代表的な遺伝毒性試験には以下の試験があります。
-
Ames(エームス)試験:
細菌を用いて遺伝毒性を検出する試験です。遺伝子が変化することを指標に遺伝毒性を検出します。 -
染色体異常試験:
動物細胞を用いて遺伝毒性を検出する試験です。染色体の形や数の変化を指標に遺伝毒性を検出します。 -
小核試験:
投与した動物の骨髄細胞(幼若赤血球)を観察して遺伝毒性を検出する方法です。細胞内に残った核の断片(小核)の数を指標に遺伝毒性を検出します。
(2)発がんプロモーション試験とは?
げっ歯類を用いた2段階発がんモデルの試験系、遺伝子改変(トランスジェニック)げっ歯類を用いた発がんモデルの試験系などがあります。
遺伝子改変動物とは、遺伝子を組み換えた動物で、本来持っていない遺伝子を組み入れた動物です。また、もともと持っている遺伝子の一部を機能しないように破壊した動物(ノックアウト動物)を含めて取り扱うこともあります。
遺伝子改変動物は毒性等の機序の解明や発がん物質の短期スクリーニングには有用な場合があるものの、定量的な用量反応データが得られないこと、これまでのところ諸外国や国際機関において十分なバリデーションが行われた試験系がないことが課題です。遺伝子改変動物は国際的にも、食品健康影響評価の参考として扱われています。
(3)発がん性(がん原性)試験とは?
例えば医薬品の場合、国際的に受け入れられているガイドラインに沿ったICHガイダンスに基づき、発がん性試験は以下の試験を行うこととされています。(「医薬品のがん原性試験に関するガイドラインの改正について」、薬生薬審発0310第1号(令和5年3月10日)各都道府県衛生主管部(局)長あて厚生労働省医薬・生活衛生局医薬品審査管理課長通知)
- 基本的な考え方は、1種のげっ歯類(ラットを推奨)を用いる長期発がん性試験に加えて、短期・中期in vivo げっ歯類試験系の1つを実施して評価を行う。
- 短期・中期in vivo げっ歯類試験系を用いたモデルについては科学的正当性を明確にする必要がある。
- 従来の2種のげっ歯類を用いての長期発がん性試験評価も容認する。
げっ歯類における医薬品のがん原性は、腫瘍の発生頻度や発生時期、ヒトとげっ歯類における薬物動態の比較、および、げっ歯類での発がんがヒトと関連するか否かについての情報が得られるような補助的研究あるいはメカニズム研究を基に評価を行います。
